로봇을 조립한다고 생각해보자. 여러 모양의 부품을 설명서에 맞춰 조립해야 할 것이다. 설명서엔 이렇게 쓰여 있다. ‘우선 1번 상자의 부품으로 팔을 만들고… 20번 상자의 부품으로 눈을 만들어 마무리한다.’ 각각의 상자에 부품이 제대로 들어갔다면 제대로 된 로봇을 만들 수 있을 것이다.
세포 안에서도 예화와 비슷한 일이 일어난다. 세포는 DNA라는 설명서에 맞춰 아미노산을 조립해 단백질을 만든다. DNA는 네 가지 ‘알파벳’ A(아데닌), G(구아닌), C(사이토신), T(싸이민)의 배열로 이뤄진다. 예컨대 ATGGAG로 이뤄진 DNA는 ATG 상자와 GAG 상자에서 아미노산 하나씩 꺼내 연결하라는 의미다. 여기서 각각의 상자에 알맞은 아미노산을 넣는 작업은 ARS(Aminoacyl-tRNA Synthetase)라는 효소가 진행한다. 이런 식으로 아미노산을 수백에서 수천 개까지 연결하면 단백질이 형성된다.
ARS가 발견된 지 오랜 시간이 흘렀지만 위의 기능 외에 알려진 다른 기능은 없었다. 하지만 김성훈 교수(융합과학기술대학원)는 수십년의 연구 끝에 ARS가 암을 비롯한 질병 발생에 관여하는 등 수많은 역할을 한다는 사실을 밝혔다. 김 교수는 연구의 중요성을 인정받아 지난달 호암재단에서 시상하는 호암상 의학상 수상자로 선정됐다.

▲ 호암상 의학상을 수상한 김성훈 교수가 본인의 연구 내용을 설명하고 있다.
사진: 유승의 기자 july2207@snu.kr
김 교수는 ARS가 단백질 합성뿐 아니라 세포의 다양한 반응에 참여해 ‘ARS 네트워크’를 이룬다는 사실을 밝혔다. 그는 다양한 반응 중에서도 ARS가 암을 일으키는 두 가지 기작에 특히 주목했다. 우선 ARS의 주된(canonical) 기능, 즉 아미노산을 상자에 담는 기능이 암 발생과 연관된다. 암은 세포가 분열을 주체하지 못해 암 덩어리를 만드는 질병인데 암세포가 빨리 분열하려면 단백질이 빨리 합성돼야 한다. 이를 위해 ARS는 단백질 합성에 필요한 아미노산을 더 빨리 상자에 담아야 한다. 김 교수는 이렇게 ARS의 활성화가 암 발생에 필수적인 조건인 점을 역이용해 암 치료의 방법을 개발할 수 있다고 봤다. 그는 “ARS 활성을 억제해 단백질 합성을 방해함으로써 암의 확산을 막을 수 있다”고 밝혔다.
ARS의 부가적인(non-canonical) 기능 또한 암 발생과 관련이 있다. 세포가 암과 관련된 위험을 감지하면 ARS는 세포 밖으로 분비돼 다양한 반응을 일으킨다. 일례로 글라이신(glycine)이라는 아미노산을 상자에 담는 ARS인 GRS(Glycyl-tRNA Synthetase)가 있다. 백혈구의 일종인 대식세포는 암세포가 방출하는 신호물질인 Fas를 인지하여 GRS를 분비한다. GRS는 암세포에 결합한 뒤 이를 파괴해서 암을 억제하는 역할을 한다. 이런 과정이 제대로 진행되지 않으면 암세포를 억제하기 어렵게 된다.(그림①)
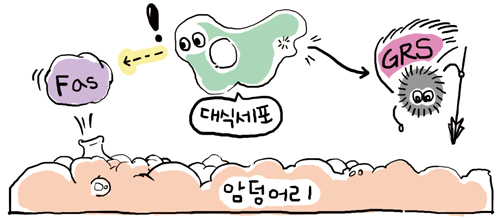
삽화: 이철행 기자 will502@snu.kr
암 발생에는 ARS뿐 아니라 ARS의 ‘친구’도 관여한다. 포유류 세포에서 ARS에 붙어 다니는 단백질인 AIMP(ARS-Interacting Multifunctional Protein)도 암 발생에 중요한 역할을 한다. 김 교수는 AIMP가 암 발생을 억제하는 기작을 최초로 밝혔다. 예컨대 AIMP3가 DNA 손상을 감지하면 p53이라는 단백질을 활성화하는데, p53은 DNA 손상을 고치도록 돕는다. 만약 AIMP3가 망가지면 세포가 DNA 손상에 취약해져 암세포로 전환될 수 있다. 실제로 김 교수의 연구에 따르면 AIMP3이 망가진 쥐는 출생 후 15개월 정도에 유방암을 비롯한 각종 암에 걸린다.(그림②)
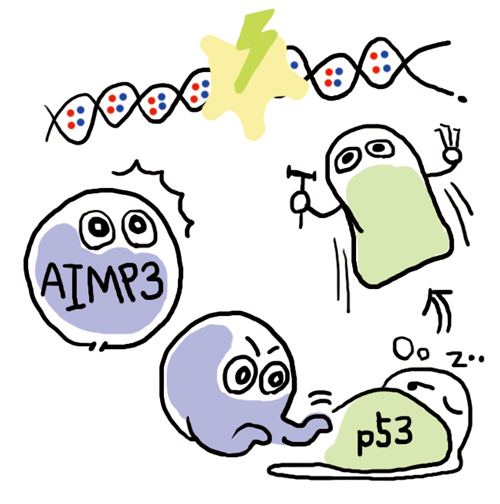
▲ AIMP3는 DNA손상을 인지하면 p53을 활성화한다. 활성화된 p53은 DNA 복구를 돕는다.
삽화: 이철행 기자 will502@snu.kr
이외에도 ARS는 면역 반응에 관여하는 등 중요한 기능을 담당한다. 하지만 이런 중요성에도 불구하고 김 교수 이전의 ARS에 대한 연구는 지금처럼 활발하지 않았다. 그 이유로 김 교수는 “과거 연구자들은 ARS 연구가 모두 완성됐다고 생각했다”는 학계의 인식을 문제점으로 짚었다. 많은 연구자들은 ARS가 아미노산을 알맞은 상자에 분류한다는 것만 밝히고 그것이 ARS 기능의 전부라고 여겨 더 이상 연구를 진행하지 않은 것이다. 그는 “ARS는 생명체가 만든 최초의 효소이자 가장 중요한 효소”라며 “이 중요한 효소가 기능을 하나만 가지고 있다는 인식에 불만을 갖고 ARS 연구를 시작했다”고 말했다.
심화된 연구를 가로막던 기술적 장벽들이 해결되며 김 교수의 ARS 연구도 진척을 보였다. 인간의 DNA를 분석하는 ‘인간 유전체 프로젝트’(Human Genome Project)는 ARS가 더 다양한 기능을 수행할 수 있다는 가능성을 제시했다. 현미경 기술의 발달도 주효했다. ARS가 이동한다거나 세포 밖으로 분비된다는 사실은 발달된 형광현미경을 통해 관찰할 수 있었다. 이렇게 관찰한 세포 수준의 반응이 실제 생체에서 어떻게 나타나는지 확인하는 데는 실험쥐 조작 기술이 기여했다. 김 교수는 “2003년 네이처에 발표한 내 연구가 우리나라에서 처음으로 유전자 조작 쥐를 사용한 연구일 것”이라 말하기도 했다.
김 교수는 수십년의 연구 끝에 ARS의 여러 기능을 증명했고 나아가 이제는 그것이 유의미함을 밝히는 과제를 남겨두고 있다. 김 교수는 “(ARS 연구가) ‘인간 복지와 건강에 어떤 기여를 할 수 있나’ 라는 도전이 남아있다”며 현재는 ARS의 의약학적 응용 분야에 대한 연구를 진행하고 있다고 밝혔다. 특히 김 교수가 매진하고 있는 분야는 항암제 개발이다. ARS의 일탈이 암을 일으키는 원인이라면 그 일탈을 억제하는 항암제 개발에 ARS 연구 성과를 응용할 수 있다.
다만 그는 “중요한 발견이 반드시 질병을 치료하는 것으로 연결되지는 않는다”며 “만 개의 발견 중 하나가 환자를 치료한다”고 신약 개발의 어려움을 표했다. 설사 그가 항암제를 개발하더라도 “하나의 칼을 제공하는 것에 그칠 뿐” 암이 발생하는 기원은 다양하기 때문에 암을 완치할 수는 없다는 게 그의 설명이다.
앞이 보이지 않는 연구를 하면 불안하지 않느냐는 기자의 질문에 그는 “선배들이 수많은 불확실성에 도전해 대한민국이 여기까지 온 것”이라고 답했다. 그는 “그중에서도 내가 가장 어려운 영역을 맡아야 하지 않겠냐”며 미소지었다. 지식의 발견에만 만족하지 않고 나아가 사회를 보다 이롭게 발전시키겠다는 도전. 그의 행보를 앞으로도 기대한다.